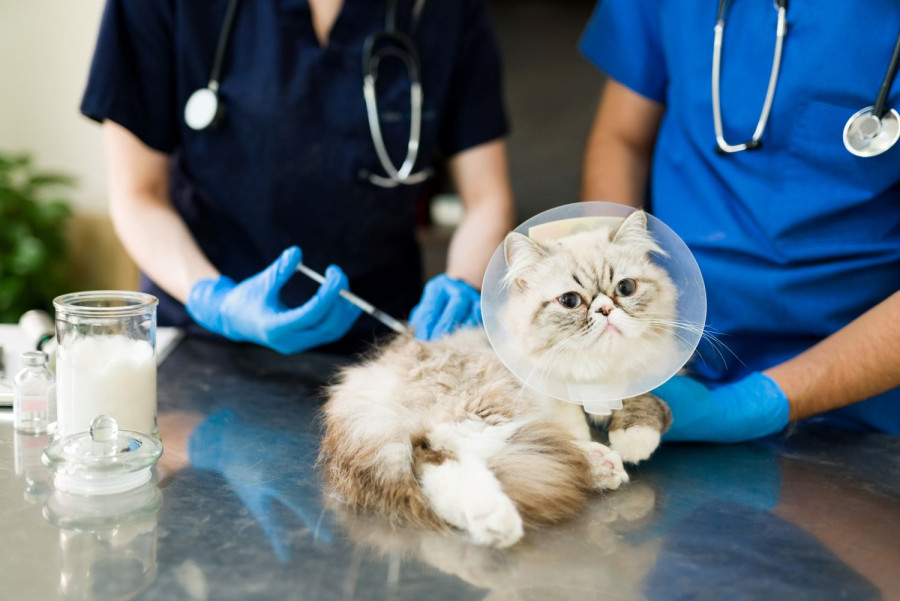
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) συνέστησε τη χορήγηση άδειας κυκλοφορίας στην Ευρωπαϊκή Ένωση για το Nobivac NXT HCPChFeLV, ένα εμβόλιο για την προστασία των γατών από κοινές λοιμώδεις ασθένειες.
Το εμβόλιο στοχεύει πέντε παθογόνους οργανισμούς:
- τον ιό του έρπητα των γατών τύπου 1, έναν ιδιαίτερα μεταδοτικό ιό που προκαλεί νόσο του ανώτερου αναπνευστικού και των ματιών,
- τον καλικιό ιό των γατών, επίσης πολύ μεταδοτικό, που προκαλεί νόσο του ανώτερου αναπνευστικού και της στοματικής κοιλότητας,
- τον ιό της πανλευκοπενίας των γατών, που μπορεί να προκαλέσει διάρροια, εμετούς, πυρετό και λήθαργο και μπορεί να αποβεί θανατηφόρος, ιδιαίτερα σε γατάκια,
- τον ιό της λευχαιμίας των γατών, που καταστέλλει το ανοσοποιητικό σύστημα και αποτελεί συχνή αιτία καρκίνου στις γάτες,
- το βακτήριο Chlamydia felis, που προκαλεί κυρίως λοιμώξεις στα μάτια.
Το εμβόλιο περιέχει ζωντανά εξασθενημένα στελέχη των παραπάνω παθογόνων (έρπητα τύπου 1, καλικιό ιού, πανλευκοπενίας και Chlamydia felis). Τα εξασθενημένα αυτά στελέχη ενεργοποιούν το ανοσοποιητικό σύστημα και βοηθούν τον οργανισμό να αναγνωρίζει τους μικροοργανισμούς και να αντιδρά γρήγορα και αποτελεσματικά σε μελλοντική έκθεση.
Για τον ιό της λευχαιμίας των γατών, το εμβόλιο περιέχει επίσης αυτοενισχυόμενο RNA (self-amplifying RNA), το οποίο είναι ενσωματωμένο σε ένα ιικό σωματίδιο χωρίς δυνατότητα αναπαραγωγής. Το σωματίδιο αυτό μεταφέρει το RNA στα κύτταρα, επιτρέποντας την παραγωγή μιας πρωτεΐνης του ιού που ενεργοποιεί την ανοσολογική απόκριση και προετοιμάζει τον οργανισμό για μελλοντική επαφή με τον ιό.
Το Nobivac NXT HCPChFeLV είναι το πρώτο κτηνιατρικό εμβόλιο που συνιστάται για έγκριση στην ΕΕ και περιέχει αυτοενισχυόμενο RNA ως δραστική ουσία.
Ανοσολογική απόκριση και συμπτώματα
Για την αξιολόγηση της ασφάλειας και της αποτελεσματικότητας, η επιτροπή κτηνιατρικών φαρμάκων (CVMP) του EMA εξέτασε δεδομένα από 15 μελέτες σε ελεγχόμενες συνθήκες και μία επιτόπια μελέτη σε 142 γάτες υπό καθημερινές συνθήκες.
Τα δεδομένα έδειξαν ότι το εμβόλιο προκαλεί επαρκή ανοσολογική απόκριση έναντι και των πέντε παθογόνων, με την ανοσία να ξεκινά περίπου μία εβδομάδα μετά τον εμβολιασμό. Η διάρκεια της ανοσίας είναι:
- 3 έτη για τον ιό της πανλευκοπενίας
- 1 έτος για τα υπόλοιπα τέσσερα παθογόνα
Οι μελέτες έδειξαν ότι το εμβόλιο προσφέρει τα εξής κλινικά οφέλη:
- μείωση της θνησιμότητας, των συμπτωμάτων και της μετάδοσης του ιού του έρπητα τύπου 1,
- μείωση των συμπτωμάτων και της μετάδοσης του καλυκοιού,
- πρόληψη της θνησιμότητας και των συμπτωμάτων της πανλευκοπενίας, καθώς και της λευκοπενίας και της μετάδοσης του ιού,
- μείωση των συμπτωμάτων και της μετάδοσης του Chlamydia felis,
- μείωση των συμπτωμάτων της λευχαιμίας των γατών και της ιαιμίας (παρουσία του ιού στο αίμα).
Ανεπιθύμητες ενέργειες
Το εμβόλιο είναι γενικά καλά ανεκτό. Οι πιο συχνές ανεπιθύμητες ενέργειες (σε 1 έως 10 στις 100 γάτες) είναι οίδημα στο σημείο της ένεσης και πυρετός, τα οποία διαρκούν περίπου μία ημέρα – αντιδράσεις που είναι συνηθισμένες για τα περισσότερα εμβόλια.
Επιπλέον, θεωρείται ασφαλές για τον άνθρωπο που το χορηγεί και για το περιβάλλον, όταν χρησιμοποιείται σύμφωνα με τις οδηγίες.
Η διαδικασία παραγωγής και οι έλεγχοι ποιότητας κρίθηκαν επαρκείς για τη διασφάλιση σταθερής ποιότητας του εμβολίου.
Η επιτροπή CVMP κατέληξε ότι τα οφέλη του Nobivac NXT HCPChFeLV υπερτερούν των κινδύνων. Η σύσταση για έγκριση θα αποσταλεί τώρα στην Ευρωπαϊκή Επιτροπή, η οποία θα λάβει την τελική, νομικά δεσμευτική απόφαση για όλη την Ευρωπαϊκή Ένωση.